Diabète sucré
[?] Qu'est-ce que c'est ?
Le diabète sucré est une affection caractérisée par l'augmentation du taux de sucre dans le sang (i.e. la glycémie) lié à
un mauvais fonctionnement de l'insuline ou à une absence d'insuline. L'insuline est une hormone qui fait baisser la glycémie. Pour comprendre le diabète, quelques notions de physiologie sont
nécessaires.
Quelques notions de physiologie : l'insuline et la régulation de la glycémie
Le glucose est le nutriment essentiel des cellules. A tout instant, il est consommé par les différents tissus pour assurer
le maintien de la température du corps, réagir à l'activité physique ou nourrir la cellule cérébrale...
Le taux
de sucre dans le sang est remarquablement fixe chez l'individu normal ; il fluctue entre 0,7 et 1,10 g/l à jeun. Cet équilibre est essentiellement sous la dépendance de
l'insuline.
L'insuline est sécrétée par des cellules du pancréas endocrine, à savoir les cellules ß (bêta) des
îlots de Langerhans. Elle régule le taux de glucose dans le sang.
D'où vient le glucose sanguin ?
Il existe deux sources de glucose sanguin : le glucose endogène et le glucose exogène. Le glucose endogène provient :
-
Des glucides de réserve, stockés sous forme de glycogène dans le foie et les muscles ;
-
Des triglycérides stockés dans le tissu adipeux sous forme de graisse.
Le glucose exogène. Il correspond à tous les glucides absorbés lors de l'alimentation. La massivité et la soudaineté de ces
apports provoqueraient une élévation brutale de la glycémie si l'organisme n'était pas capable de stocker rapidement, sous forme de réserve, ces glucides alimentaires dans le foie, puis dans la
graisse et les muscles. Ce stockage se fait dans l'heure qui suit le repas.
Le foie est la plaque tournante du métabolisme glucidique et le carrefour des flux de glucose endogène et exogène. Quant à
l’insuline, elle régule ces flux de glucose.
Le pancréas sécrète l'insuline de façon très particulière :
Régulation de la sécrétion pancréatique
La sécrétion pancréatique d'insuline obéit à plusieurs règles et est constamment contrôlée. Toute augmentation de la glycémie entraîne une augmentation de la production d'insuline et donc une diminution de la libération du
glucose hépatique. A l'inverse, toute diminution de la glycémie entraîne une diminution de la production d'insuline et donc une augmentation de la libération du glucose hépatique.
Par ailleurs, des facteurs centraux et digestifs interviennent également dans le contrôle de la sécrétion d’insuline. Par
l'intermédiaire du système nerveux central et des hormones digestives, l'alimentation provoque une production anticipatoire d'insuline. Cette dernière empêche la survenue d'une trop forte
hyperglycémie postprandiale. On parle alors de l’effet "anti-hyperglycémiant" de l'insuline puisque l'augmentation de la sécrétion ne sert pas à corriger l'hyperglycémie induite par le repas mais
à prévenir l'ascension glycémique qui pourrait découler de cette prise alimentaire.
Mode d'action de l'insuline
L'insuline exerce son effet au niveau des cellules-cibles hépatiques, musculaires et adipeuses au cours de deux phases
successives.
Tout d'abord, l'insuline se lie à des récepteurs membranaires spécifiques, les glycoprotéines, présents à la surface de la
membrane cellulaire. Ceux-ci " reconnaissent " l’insuline , la fixent et créent un complexe insulino-récepteur. Se produisent alors des réactions biochimiques successives. Elles
permettent l'action intra-cellulaire de l'insuline à partir de cette fixation membranaire.
L'intégrité fonctionnelle de ces étapes membranaire et intra-cellulaire est indispensable au maintien d'une glycémie
stable. L'effet périphérique de l'insuline dépend du nombre et de l'affinité des récepteurs de l'insuline qui sont influencés par de nombreux facteurs, en particulier le poids. Toute obésité
entraîne une diminution du nombre des récepteurs et de l'action périphérique de l'insuline. Ce phénomène est appelé " état d’insulinorésistance ".
Les origines du diabète
Il existe deux types de diabète :
-
Les diabètes secondaires ;
-
Le diabète dit "essentiel" qui se divise en :
- Diabète insulinodépendant (DID) ou de type 1 ;
- Diabète non insulinodépendant (DNID) ou de type 2
Les diabètes secondaires
Les causes sont multiples :
-
Les causes pancréatiques : pancréatectomie, pancréatite chronique, cancer du pancréas, hémochromatose...
-
Les causes endocriniennes : hypersécrétion d'une hormone hyperglycémiante (acromégalie, syndrome de Cushing,
phéochromocytomes...) ou inhibition de l'insulinosécrétion (syndrome de Conn avec hypokaliémie) ;
-
Les causes iatrogènes : corticoïdes, oestrogènes, diurétiques hypokaliémiants...
-
Les syndromes génétiques : trisomie 21, Turner, Klinefelter...
-
Les diabètes nutritionnels de 3ème type observés dans certains pays du tiers-monde.
Le diabète essentiel :
voir le chapitre correspondant
[?] Examens et analyses complémentaires
La glycémie est généralement dosée à partir de sang veineux prélevé chez un sujet à jeun depuis au moins 8
heures. La glycémie postprandiale est pour sa part dosée 2 heures après un repas normal.
L'hyperglycémie provoquée par voie orale (HGPO) mesure la glycémie toutes les 30 minutes, pendant 3 à 5 heures, après
absorption de 75 g de glucose. Il est nécessaire d'avoir un régime normalement glucidique dans les deux ou trois
jours avant l'examen. Cette épreuve biologique n’est guère utilisée, hormis pour la grossesse.
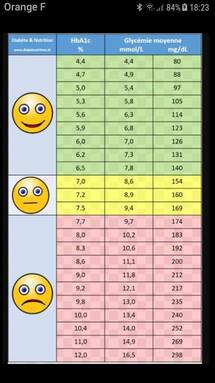
L'hémoglobine glyquée, ou glycosylée, HbA1C, est une partie de l'hémoglobine normale qui fixe de façon presque irréversible
le glucose sanguin en fonction de pics d'hyperglycémie. Elle reflète donc l'équilibre glycémique des deux à trois mois précédents. Le taux moyen est de 5,4%. Il doit rester inférieur à 7% chez un
diabétique traité.
Le dosage radio-immunologique de l'insuline plasmatique ou du peptide C circulant est possible. Le peptide C est le
constituant initial de la pro-insuline et est sécrété en même temps, et dans la même quantité, que l'insuline. Il permet une appréciation de la sécrétion d'insuline chez un diabétique traité par
insuline injectable.
Le médecin parle de diabète lorsque la glycémie à jeun est supérieure ou égale à 1,26 g/l (7 mmol/l) ou lorsque la glycémie
est supérieure à 2g/l (11 mmol/l) quel que soit le moment de la journée
Complications du diabète
a) Métaboliques
Le coma acido-cétosique avec hyperglycémie apparaît en cas de déficit sévère en insuline. Il complique le diabète de type
1nsulinodépendant le plus souvent. L'acidocétose peut révéler le diabète ou survenir à l'occasion d'une erreur thérapeutique ou d'une complication intercurrente. La polyurie et la polydipsie sont
majorées; des nausées, des vomissements et des douleurs abdominales peuvent égarer le diagnostic. La déshydratation est constante. Il y a évolution vers des troubles de la conscience et vers le
coma. Le diagnostic de certitude se fait d’après les urines (glycosurie, acétonurie), celui de gravité s’établit grâce au dosage de la glycémie. Le traitement fait appel à la réhydratation,
l'alcalinisation et l'insulinothérapie intraveineuse continue. Le plus souvent, le pronostic est bon.
Le coma hyperosmolaire concerne surtout le sujet âgé, le plus souvent diabétique de type non insulinodépendant. A
l'occasion d'un déficit hydrique, des troubles de la conscience s'installent alors qu’apparaît une importante déshydratation. Le diagnostic repose sur l'hyperosmolarité sanguine avec
hyperglycémie supérieure à 6 g/l et natrémie (taux de sodium) supérieure à 150 mmol/l sans cétose. Le traitement repose sur la réhydratation et l'insulinothérapie. La mortalité est
malheureusement élevée, de l'ordre de 50%.
L'acidose lactique est souvent consécutive à une erreur thérapeutique: par exemple lors d’une prescription de biguanides à
un diabétique présentant une contre-indication (insuffisance rénale, insuffisance hépatique, insuffisance cardio-respiratoire...). Les troubles de la conscience et l'anurie dominent le tableau.
Le diagnostic repose sur l'acidose métabolique avec trou anionique, l'absence de cétose et l’hyperglycémie modérée. Le traitement se fonde sur l'alcalinisation et la réhydratation en milieu
spécialisé. Cependant, la mortalité reste de 60%.
L'hypoglycémie est une complication fréquente. Ses symptômes doivent être connus :
-
Pâleur, transpiration, tachycardie ;
-
Fatigabilité, troubles de l'humeur, diplopie (le sujet " voit double ") ;
-
Convulsion, agitation psychomotrice, signes évoquant une ivresse alcoolique aiguë ;
-
Coma.
Les causes d'hypoglycémies sont multiples. Dans le DID, il s'agit d'une inadéquation entre le régime alimentaire,
l'activité physique et la dose d'insuline. Dans le DNID, il peut s'agir d'interactions médicamenteuses avec un sulfamide hypoglycémiant (sulfamide anti-bactérien, antivitamine K, aspirine,
certains AINS) ou de tares viscérales surajoutées (insuffisance rénale).
Le traitement de l'hypoglycémie repose sur l'administration de sucre sous plusieurs formes :
b) Les complications dégénératives : microangiopathies et macroangiopathies
L'atteinte des gros vaisseaux (la macroangiopathie) :
Le diabète fait partie des facteurs de risque vasculaire et multiplie par deux ou trois le risque d'accidents
cardiovasculaires. Ceux-ci causent de 75% des décès chez le diabétique : angine de poitrine, infarctus du myocarde, artériopathie des membres inférieurs, accidents vasculaires cérébraux. Les
autres facteurs de risque doivent être pris en compte dans le traitement : obésité, hypertension artérielle, dyslipidémie (hypercholestérolémie), tabagisme...
L'atteinte des petits vaisseaux (la microangiopathie) : L'atteinte des vaisseaux de petit calibre et des capillaires est
relativement spécifique au diabète. La sévérité et la durée de l'hyperglycémie jouent un rôle de même que l'hypertension artérielle et le tabagisme.
La rétinopathie diabétique est l'une des principales complications du diabète. Le diabète est en effet la première cause de
cécité dans le monde occidental. La moitié des diabétiques présentent une maladie de la rétine après 15 ans d'évolution. En terme de gravité, les médecins distinguent plusieurs stades depuis la
rétinopathie plane "non proliférante" jusqu'à la rétinopathie proliférante qui ne survient heureusement que chez 10% des diabétiques. La rétinopathie non proliférante se manifeste par une baisse
de l'acuité visuelle. La rétinopathie proliférante est caractérisée par la prolifération de néovaisseaux fragiles qui provoquent des troubles sévères : hémorragie rétinienne, décollement de
rétine, glaucome vasculaire.
Le traitement comprend deux volets :
-
L'équilibration optimale du diabète retarde la survenue et l'aggravation de la rétinopathie au stade non prolifératif et
peut améliorer l'oedème maculaire; c'est dire l'importance de la surveillance et de l'équilibration du diabète ;
-
Le traitement ophtalmologique par photocoagulation au laser vise à supprimer les zones ischémiées.
Une consultation ophtalmologique est nécessaire tous les ans pour le patient diabétique. L'angiofluorographie (angiographie
à la fluorescéine) fait partie de la surveillance régulière car cet examen précise les lésions, les troubles de la perfusion, leur évolution et les indications thérapeutiques. Il s'agit
d'injecter dans une veine du bras de la fluorescéine et de regarder au fond d'oeil à travers des filtres spéciaux ce qui se passe. En cas de lésion des vaisseaux, le colorant exsude à travers les
parois et des images très précises sont ainsi obtenues.
La néphropathie diabétique est la complication rénale du diabète. Elle est définie par une protéinurie, une tendance à
l'hypertension artérielle et une détérioration progressive de la fonction rénale. L'insuffisance rénale chronique atteint à long terme la moitié des diabétiques (DID).
La néphropathie diabétique débutante est le stade primordial vers lequel toute l'attention se tourne actuellement. Elle est
définie par une microalbuminurie (0,03 à 0,3 g/jour d'albumine urinaire). Cette microalbuminurie est un indice prédictif d'évolution vers la néphropathie diabétique patente chez les DID et de
complications cardiovasculaires chez les DNID. La microalbuminurie permet de définir une population à risque sur laquelle tous les effets thérapeutiques doivent se porter. Le traitement
insulinique optimisé a des effets bénéfiques probables. Le traitement antihypertenseur précoce diminue l'excrétion urinaire d'albumine et retarde l'évolution vers l'insuffisance rénale.
c) La neuropathie diabétique
Elle a des expressions très diverses :
-
La neuropathie périphérique touche les membres inférieurs ; elle est à prédominance sensitive : le patient
présente des troubles de la sensibilité à la chaleur et à la douleur ; il perçoit mal les vibrations du diapason. Les réflexes ostéo-tendineux (ROT) sont diminués ou abolis. Ces troubles
sensitifs prédisposent à l'ostéoarthropathie et au mal perforant plantaire ;
-
La mononeuropathie s'exprime par l'atteinte d'un seul nerf : diplopie par atteinte d'un nerf moteur oculaire,
paralysie faciale périphérique...
-
L'atteinte du système nerveux végétatif se traduit par des troubles digestifs (gastroparésie, diarrhée), urinaires
(troubles de la vidange vésicale, impuissance, éjaculation rétrograde), vasculaires (hypotension orthostatique) et par la disparition des symptômes d'origine adrénergique des hypoglycémies
(pâleur, sueurs, tachycardie...).
Sa prévention passe par un bon équilibre de la glycémie.
Le traitement fait appel :
-
Aux antidépresseurs et à la carbamazépine pour les douleurs ;
-
A la kinésithérapie en cas d'atteinte motrice ;
-
Aux antidiarrhéiques et prokinétiques dans les troubles digestifs...
d) les infections
Le diabète mal équilibré favorise les infections bactériennes et mycosiques qui elles-mêmes déséquilibrent le diabète. Sont
particulièrement fréquentes : les infections urinaires et les infections cutanées à staphylocoques ou à champignons (mycoses).
e) le pied du diabétique
Il est caractérisé par la surinfection de plaies négligées, des troubles circulatoires et des maux perforants.
Les causes sont intriquées : ischémie, neuropathie périphérique (perte de sensibilité), neuropathie végétative (troubles
circulatoires locaux favorisant l'ostéoarthropathie). L'infection est un facteur aggravant des lésions ischémiques et neuropathiques. La prévention est primordiale : hygiène des pieds, chaussures
non traumatisantes, soins de pédicure remboursés par la Sécurité Sociale pour les diabétiques (ablation de callosités et coupe non traumatique des ongles).

Un membre de votre entourage ou vous-même venez d'apprendre le diagnostic. Vous avez envie d'échanger vos points de vue
avec d'autres personnes dans votre cas. Parler du diabète n'est pas toujours facile, Forum nos forums vous sont
ouverts.
Dr Lyonel Rossant, Dr Jacqueline
Rossant-Lumbroso.

 Forum Santé
Forum Santé
http://www.doctissimo.fr/html/sante/encyclopedie/sa_1289_diabete_sucrechar.htm



























 Nicolas Lefrançois, 28 ans, ex-champion de Normandie de… boxe (moins de 86 kilos) et
Nicolas Lefrançois, 28 ans, ex-champion de Normandie de… boxe (moins de 86 kilos) et  le Breton Corentin Cherhal, 21 ans
le Breton Corentin Cherhal, 21 ans



 Nom commun : Aneth, Aneth odorant, Faux anis, Fenouil bâtard
Nom commun : Aneth, Aneth odorant, Faux anis, Fenouil bâtard














 Propriétés et indications de l'huile essentielle d'angélique
Propriétés et indications de l'huile essentielle d'angélique









 www.grandfrais.com/valeurs/valeurs-1-112.html
www.grandfrais.com/valeurs/valeurs-1-112.html 
 Abbott SA / NV
Abbott SA / NV

































































































 On estime que la cataracte atteint plus d’une personne sur cinq à partir de 65 ans, plus d’une sur trois à partir de
75 ans et près de deux sur trois à partir de 85 ans. Cette affection est due au développement d’opacités sur le cristallin, la lentille transparente qui permet l'accommodation. Ces
opacités empêchent les rayons lumineux de passer, entraînant une diminution de la vision qui peut être très importante.
On estime que la cataracte atteint plus d’une personne sur cinq à partir de 65 ans, plus d’une sur trois à partir de
75 ans et près de deux sur trois à partir de 85 ans. Cette affection est due au développement d’opacités sur le cristallin, la lentille transparente qui permet l'accommodation. Ces
opacités empêchent les rayons lumineux de passer, entraînant une diminution de la vision qui peut être très importante. Les
Les  Aucun traitement ne permet de guérir le
diabète. C'est une
Aucun traitement ne permet de guérir le
diabète. C'est une 

