S45
LA RÉTINOPATHIE DIABÉTIQUE
A-P. Guagnini, B. Snyers
Mots-clefs : diabète, rétinopathie, maculopathie,
classification, facteurs de risque, traitement
INTRODUCTION
La rétinopathie diabétique (RD) est une des premières causes
de cécité dans les pays industrialisés pour les patients de moins de soixante ans . On estime qu’après quinze ans de diabète près de 2% des diabétiques sont aveugles et 10% sont
malvoyants.
La malvoyance est en général liée aux complications de la
rétinopathie diabétique proliférante chez les diabétiques de type 1 et est souvent secondaire à la maculopathie diabétique chez les patients diabétiques de type 2.
La prévalence de la rétinopathie diabétique augmente avec
l’ancienneté du diabète et chez les patients traités par insuline (1, 2, 3).
Les études épidémiologiques montrent que, outre l’ancienneté
du diabète, l’hyperglycémie chronique, l’hypertension artérielle, l’hypercholestérolémie, la protéinurie et certaines situations hormonales telles que la grossesse et la puberté sont des facteurs
de risque reconnus dans la progression de la rétinopathie diabétique et de la maculopathie diabétique (1,2,4,5).
Face à cette menace de RD invalidante, le défi consiste en un
dépistage efficace des patients à risque, en une prévention et un contrôle des facteurs de risque et en une prise en charge précoce des complications rétiniennes. La communication entre le
médecin traitant, l’endocrinologue et l’ophtalmologue est donc essentielle pour assurer au patient diabétique un meilleur pronostic visuel.
PHYSIOPATHOLOGIE
DE LA RÉTINOPATHIE DIABÉTIQUE
L’élévation chronique du glucose sanguin aboutit, via des
réactions biochimiques non encore tout à fait élucidées mais impliquant le rôle toxique des polyols produits à partir d’un excès de glucose et le rôle des anomalies hématologiques associées, à
l’apparition de lésions histologiques et d’anomalies du flux sanguin au niveau des capillaires rétiniens, à la rupture de la barrière hématorétinienne et à l’apparition de néovascularisations
rétiniennes.
Les lésions histologiques consistent en un épaississement de
la membrane basale des capillaires rétiniens, et en la disparition des péricytes à leur niveau avec pour conséquence une dilatation et une occlusion des capillaires et l’apparition de
microanévrismes. L’occlusion des capillaires rétiniens est également liée à une leucostase anormale.
La rupture de la barrière hématorétinienne consiste au
passage anormal de constituants plasmatiques dans la rétine via l’ouverture de jonctions serrées entre les cellules endothéliales et est favorisée par la présence de lésions histologiques et la
présence de VEGF (vascular endothelial growth factor).
L’occlusion des capillaires mène à l’apparition de
territoires de non-perfusion rétinienne qui synthétisent différents facteurs de croissance dont le VEGF. Ainsi, on assiste au développement de proliférations néovasculaires.
CLASSIFICATION DE LA RÉTINOPATHIE DIABÉTIQUE
Effectuer une classification de la rétinopathie diabétique
est primordial car c’est ce qui va permettre d’établir un fil de conduite pour le suivi et le traitement du patient.
Il existe de nombreuses classifications, dont la plus
consensuelle est la classification de l’Early Treatment Diabetic Retinopathy Study (ETDRS) (6,7,8). Elle est basée sur différents signes découverts au fond d’oeil et leur étendue :
microanévrismes, hémorragies rétiniennes, anomalies microvasculaires intra-rétiniennes, anomalies veineuses, nodules cotonneux, exsudats durs, épaississement rétinien et proliférations
néovasculaires.
On applique aujourd’hui la classification de l’ALFEDIAM qui
est dérivée de celle de l’ETDRS et est plus simple pour la communication entre les différents spécialistes (9).
On distingue la classification de la rétinopathie diabétique
et la classification de la maculopathie diabétique :
Rétinopathie diabétique non proliférante
– RD non proliférante minime
– RD non proliférante modérée
– RD non proliférante sévère (ou RD préproliférante)
Rétinopathie diabétique
proliférante
– RD proliférante minime (néovaisseaux prérétiniens périphériques débutants)
– RD proliférante modérée (néovaisseaux prérétiniens périphériques étendus ou prépapillaires débutants)
– RD proliférante sévère (néovaisseaux prépapillaires étendus)
– RD proliférante compliquée u +/- Maculopathie diabétique
Maculopathie diabétique
– Maculopathie oedémateuse :
– oedème maculaire focal +/- exsudats
– oedème maculaire diffus – non cystoïde
– cystoïde
– Maculopathie
ischémique
FORMES CLINIQUES PARTICULIÈRES
Rétinopathie diabétique et hypertension artérielle
La rétinopathie hypertensive vient compliquer la rétinopathie
diabétique avec décompensation de la maculopathie même pour des valeurs d’hypertension artérielle modérée (10). Chez ces patients, il est indispensable de viser un équilibre tensionnel à
130mmHg/80mmHg et si nécessaire faire appel à un néphrologue spécialisé.
Rétinopathie diabétique et équilibre glycémique rapide
Lors du passage à l’insuline ou à la pompe à insuline ou lors
du renforcement du traitement par insuline, on peut noter une décompensation de la rétinopathie diabétique principalement chez les patients présentant une rétinopathie diabétique non proliférante
sévère ou une rétinopathie diabétique proliférante.
Un examen ophtalmologique est à réaliser avant toute
modification du traitement hypoglycémiant ainsi que tous les trois, quatre mois qui le suivent pendant la première année. Il faudra également veiller à normaliser progressivement l’hémoglobine
glyquée.
Rétinopathie diabétique et grossesse
Il est clairement établi qu’il existe un risque de progression de la rétinopathie diabétique en
cas de grossesse surtout lorsque celle-ci n’est pas
programmée.
Celui-ci est d’autant plus important que le diabète est
ancien, que le stade de rétinopathie de départ est sévère, que la chute glycémique est importante et qu’il existe une hypertension artérielle associée.
Un examen ophtalmologique est donc à prévoir dans la mise au
point avant la grossesse ou en tous cas en début de grossesse avec suivi ophtalmologique et éventuel traitement en fonction du stade de la rétinopathie et de sa progression.
RECOMMANDATIONS POUR LE DÉPISTAGE ET LA SURVEILLANCE DES
PATIENTS
La coopération entre le médecin traitant et l’ophtalmologue
est ici de toute première importance puisqu’au delà du suivi recommandé par l’ANAES et l’ALFEDIAM, il faut gérer le suivi en fonction des découvertes faites au fond d’oeil, de leur traitement
médical ou par laser et de la réponse de la rétine. Les examens fluoangiographiques ne seront réalisés que sur base de l’examen ophtalmologique.
Dépistage de la rétinopathie diabétique
Diabète de type 1 :
– examen du fond d’œil dès la découverte du diabète,
– examen annuel du fond d’œil,
– pas de nécessité d’un examen ophtalmologique avant l’âge de 10 ans,
– examen du fond d’œil plus régulier entre 16 et 18 ans,
– examen ophtalmologique avant la grossesse ou en début de grossesse puis tous les trimestres.
Diabète de type 2 :
– examen du fond d’œil dès la découverte du diabète,
– examen annuel du fond d’œil,
– examen du fond d’œil lors du renforcement du traitement hypoglycémique,
– examen ophtalmologique lors d’une décompensation artérielle ou rénale.
Surveillance de la rétinopathie diabétique
Examen ophtalmologique annuel en cas de
:
– absence de rétinopathie diabétique,
– RD non proliférante minime,
– RD non proliférante modérée.
Examens ophtalmologiques plus rapprochés en
fonction du stade de la rétinopathie ou de la maculopathie et de leur traitement en cas de :
– RD non proliférante sévère,
– rétinopathie diabétique proliférante,
– maculopathie oedémateuse,
– rétinopathie diabétique en début de grossesse,
– décompensation artérielle ou rénale,
– équilibre glycémique rapide.
TRAITEMENT DELA RÉTINOPATHIE DIABÉTIQUE
Traitement médical
Équilibre glycémique et tensionnel
:
L’équilibre strict glycémique réduit de 54 à 75% la
progression de la rétinopathie diabétique chez les diabétiques de type 1 et de 21% chez les diabétiques de type 2.
L’équilibre strict tensionnel réduit de 34% la progression de
la rétinopathie diabétique chez les diabétiques de type 2 et de 47% la baisse d’acuité visuelle à neuf ans.
Le pronostic visuel étant en jeu, il est donc impératif de
viser :
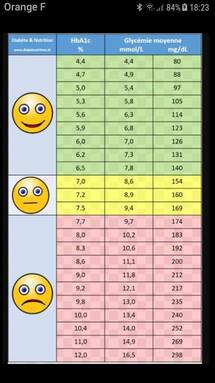
– chez les diabétique de type 1 :HbA1c ≤ 7,5%
– chez les diabétique de type 2 :HbA1c ≤ 7%TA 130mmHg/80mmHg
L’équilibre strict glycémique devra, si possible, être
réalisé de manière progressive afin d’éviter toute progression de la rétinopathie diabétique.
L’équilibre strict tensionnel doit lui être réalisé le plus
rapidement possible.
Injection intravitréenne de triamcinolone
:
La triamcinolone a des propriétés anti-inflammatoires et
anti-vasoprolifératives. Cela permet de faire diminuer et même disparaître l’œdème rétinien. Elle est donc indiquée dans la maculopathie diabétique oedémateuse diffuse rebelle. Malheureusement,
la cortisone est cataractogène et les dépôts intravitréens n’ont une durée
d’action que de quatre à six mois. Il peut également
déclencher une pathologie glaucomateuse. Ce traitement peut être répété mais doit surtout être accompagné de l’équilibre glycémique et tensionnel et d’un traitement laser approprié.
Traitement par laser
Le but du traitement est de prévenir les complications cécitantes de la rétinopathie diabétique proliférantes, à savoir l’hémorragie
intra-vitréenne, le glaucome néovasculaire et le décollement de rétine ainsi que la
baisse irréversible de la vision en cas de maculopathie diabétique oedémateuse.
Photocoagulations panrétiniennes
:
Ce traitement consiste en l’application d’impacts de laser
au niveau de la rétine située entre les arcades des vaisseaux rétiniens temporaux, la papille et l’équateur. Il est appliqué en cas de rétinopathie diabétique proliférante et de rétinopathie diabétique non proliférante sévère
(ou préproliférante). Il permet la régression des proliférations néovasculaires et prévient de l’évolution vers une rétinopathie diabétique proliférante de haut risque de baisse
d’acuité visuelle.
Photocoagulations focales ou en grid
:
Ce traitement consiste également en l’application d’impacts
de laser au niveau de la rétine de la région maculaire et seulement au niveau de zones oedémateuses qui menacent la fovéa. Il n’est réalisé qu’après l’équilibre des paramètres généraux (glycémie
et tension artérielle) car l’amélioration de ces paramètres peut voir l’oedème maculaire régresser et même disparaître.
Traitement chirurgical
Il consiste en la réalisation d’une vitrectomie parfois
associée à de l’endolaser et/ou la libération de proliférations fibrovasculaires ou épirétiniennes et rarement aussi à une cure de décollement de rétine.
Cette vitrectomie est indiquée en cas de :
– hémorragie du vitré,
– décollement de rétine par traction fibrovasculaire et traction maculaire,
– décollement de rétine mixte.
Perspectives d’avenir
À moyen terme, il sera possible de prévenir l’apparition de
proliférations néovasculaires et de les faire régresser grâce à des facteurs d’anti-vasoprolifération agissant sur le VEGF. Plusieurs molécules sont à l’essai actuellement.
CONCLUSION
La rétinopathie diabétique est une des complications les
plus invalidantes du diabète car elle menace le pronostic visuel du patient. C’est son autonomie, sa dignité et sa qualité de vie qui sont en jeu.
C’est pourquoi le dépistage et la surveillance
ophtalmologiques sont essentiels et doivent être bien gérés par les différents intervenants médicaux et acceptés et suivis par le patient lui-même. Le suivi devra être renforcé chez les patients
à risque ; c’est le cas notamment des patients qui présentent une rétinopathie diabétique non proliférante sévère ou proliférante, une maculopathie oedémateuse, c’est également vrai en cas de
grossesse, de décompensation artérielle ou rénale et d’équilibre glycémique trop rapide.
L’équilibre strict glycémique et tensionnel restent des
éléments prioritaires et complémentaires au traitement ophtalmologique symptomatique.
L’angiographie à la fluorescéine est un examen précieux pour
le dépistage et le suivi de différentes lésions rétiniennes liées au diabète mais elle n’est pas systématique et est proposée sur avis de l’ophtalmologue et en fonction de l’examen du fond
d’oeil. Il s’agit d’un examen invasif parfois compliqué de réaction allergique et qui peut rarement être compliqué d’un choc mortel.
De nouvelles thérapeutiques à visée anti-vasoprolifératives
et par injection intra-vitréenne sont attendues à moyen terme. Nous espérons qu’elles tiendront leurs promesses et offriront de nouvelles perspectives dans le traitement de la rétinopathie et
maculopathie diabétiques.
RÉFÉRENCES
1. Klein R, Klein BR, Moss SE, Davis MD, Demets DL : The Wisconcin Epidemiologic
Study of Diadetic Retinopathy :II. Prevalence and risk of diabetic retinopathy when age at diagnosis less than 30 years. Arch Ophthalmol. 1984 ; 102: 520-526.
2. Klein R, Klein BR, Moss SE, Davis MD, Demets DL: The Wisconcin Epidemiologic
Study of Diabetic Retinopathy :III. Prevalence and risk of diadetic retinopathy when age at diagnosis is 30 years or more. Arch Ophthalmol. 1984 ; 102 : 527-532.
3. Sjolie AK, Stephenson J, Aldington S, Kohner E, Janka H, Stevens L, Fuller J
and the EURODIAB complications study group: Retinopathy and vision loss in insulin-dependent diabetes in Europe. Ophthalmology. 1997; 104: 252-260.2007 ;
126, 3 : S45-49 La rhétinopathie diabétique
4. Klein R, Klein BR, Moss SE, Cruickshanks KJ: The Wisconcin Epidemiologic
Study of Diabetic Retinopathy :XIV. Ten-year incidence and progression of diabetic retinopathy when age at diagnosis is 30 years or more. Arch Ophthalmol. 1984 ; 102 :
527-532.
5. UK Prospective retinopathy from stereoscopic color fundus photographs: An
extension of the modified Airlie House Classification. ETDRS report number 10. Ophtalmology. 1991; 98: 786-806.
6. Early Treatment Diabetic Retinopathy Study research group: Grading diabetic
retinopathy from fluorescein angiograms. ETDRS report number 11. Ophtalmology. 1991; 98: 807-822.
7. Early Treatment Diabetic Retinopathy Study research group: Fundus
photographic risk factor for progression of diabetic retinopathy. ETDRS report number 12.
Ophtalmology. 1991; 98: 823-833.
8. Massin P, Angioi-Duprez K, Becin F, Cathelineau G, Chaine G et al. : Dépistage, surveillance et
traitement de la rétinopathie diabétique. Recommandations de l’ALFEDIAM. Comité d’experts ci-dessus et validé par les membre des conseils d’administration et scientifique de l’ALFEDIAM.
Diabetes Metab. 1996 ; 22 : 203-209.
9. Bresnick GH: Diabetic maculopathy. A critical review highlighting diffuse
macular oedema. Ophtalmology. 1983; 90: 1301-1317.
10. Diabetes Study (UKPDS) group: Tight blood pressure control and risk of
macrovascular and microvascular complications in type 2 diabetes; UKPDS 38. Br Med
J. 1998; 317: 703-718.
11. Early Treatment Diabetic Retinopathy Study research group .
Grading diabetic
http://www.md.ucl.ac.be/loumed/V126,%202007/mars/S45-49.pdf



























 Nicolas Lefrançois, 28 ans, ex-champion de Normandie de… boxe (moins de 86 kilos) et
Nicolas Lefrançois, 28 ans, ex-champion de Normandie de… boxe (moins de 86 kilos) et  le Breton Corentin Cherhal, 21 ans
le Breton Corentin Cherhal, 21 ans



 Nom commun : Aneth, Aneth odorant, Faux anis, Fenouil bâtard
Nom commun : Aneth, Aneth odorant, Faux anis, Fenouil bâtard














 Propriétés et indications de l'huile essentielle d'angélique
Propriétés et indications de l'huile essentielle d'angélique









 www.grandfrais.com/valeurs/valeurs-1-112.html
www.grandfrais.com/valeurs/valeurs-1-112.html 
 Abbott SA / NV
Abbott SA / NV






























































































 Le sucre n’est pas un aliment naturel important des êtres humains.
Le sucre n’est pas un aliment naturel important des êtres humains. Le sucre de canne fut et reste le premier sucre ‘produit’ et le plus important en quantité. Il est connu en Inde et en
Chine depuis probablement un millénaire avant Jésus-Christ. Des textes perses (VIème siècle avant notre ère) rapportent ‘ces roseaux qui produisent un miel sans le besoin des abeilles’. L’amiral
d’Alexandre le Grand, Niarchos (IVème siècle avant JC), en fait lui aussi mention comme le poète latin Lucain (Ier siècle de notre ère). Mais ensuite les voies du commerce se tarirent. Ce n’est
que lors de la première croisade que les Occidentaux redécouvrirent ce secret bien connu des Orientaux : ces ‘canes (sic) végétales que l’on arrose et dont on tire le sucre’ (Joinville, XIVème
siècle).
Le sucre de canne fut et reste le premier sucre ‘produit’ et le plus important en quantité. Il est connu en Inde et en
Chine depuis probablement un millénaire avant Jésus-Christ. Des textes perses (VIème siècle avant notre ère) rapportent ‘ces roseaux qui produisent un miel sans le besoin des abeilles’. L’amiral
d’Alexandre le Grand, Niarchos (IVème siècle avant JC), en fait lui aussi mention comme le poète latin Lucain (Ier siècle de notre ère). Mais ensuite les voies du commerce se tarirent. Ce n’est
que lors de la première croisade que les Occidentaux redécouvrirent ce secret bien connu des Orientaux : ces ‘canes (sic) végétales que l’on arrose et dont on tire le sucre’ (Joinville, XIVème
siècle).









